Co się odwlecze, to może… odwlec się jeszcze bardziej. W połowie grudnia ubiegłego roku giełdowe notowania Mabionu mocno ucierpiały, gdy Europejska Agencja Leków (EMA) nie wydała oczekiwanej przez rynek pozytywnej opinii dotyczącej rejestracji leku MabionCD20 na rynku unijnym. Zamiast tego polska spółka dostała kolejny zestaw pytań, na które musi odpowiedzieć. Tymczasem pod koniec stycznia pozytywną opinię EMA uzyskał z konkurencyjnym produktem koncern Pfizer.
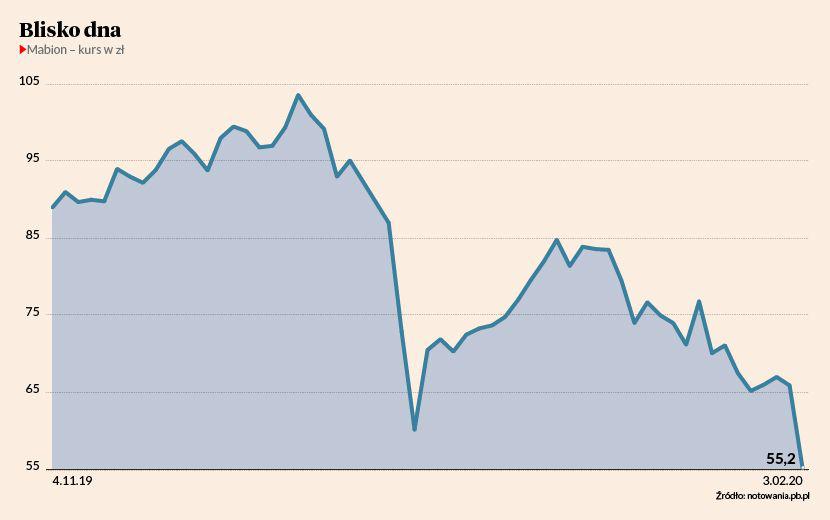
Podczas poniedziałkowej sesji kurs Mabionu znów spadał o ponad 7 proc., a notowania wróciły do poziomu z połowy grudnia. Tak nisko jak wczoraj i w połowie grudnia nie były od wiosny 2016 r. MabionCD20 jest flagowym produktem polskiej spółki. To lek biopodobny do wprowadzonego na rynek ponad dwie dekady temu przez koncern Roche rytuksymabu, wykorzystywanego m.in. w leczeniu chłoniaków i reumatoidalnego zapalenia stawów. Jego roczna sprzedaż wynosi około 7 mld USD. Po wygaśnięciu patentu Roche’a liczne firmy zaczęły pracować nad wprowadzeniem na rynek leków, które naśladują jego mechanizm działania.
By lek mógł być sprzedawany na rynku unijnym, niezbędna jest pozytywna rekomendacja EMA i zgoda Komisji Europejskiej. Dwie firmy już przeszły tę procedurę — koreański Celltrion oraz Sandoz ze szwajcarskiej grupy Novartis. Teraz najważniejszy krok w ramach procesu rejestracyjnego jest już za Pfizerem — tym samym Pfizerem, którego spółkazależna połączyła się w ubiegłym roku z firmą Mylan. Ta zaś jeszcze w 2016 r. podpisała umowę z Mabionem, na mocy której ma dystrybuować MabionCD20. W kolejce do rejestracji jest też podobny lek koncernu Amgen. Tymczasem Mabion zalicza opóźnienie.
„Spółka podkreśla, iż EMA dysponuje wieloma narzędziami zapewniającymi swobodę decyzyjną i możliwość indywidualnego dostosowania rozwiązania do potrzeb występujących w danej procedurze rejestracyjnej. Spółka nie ma wpływu na ocenę EMA. Istnieje wiele możliwych zdarzeń — wydanie decyzji pozytywnej bądź negatywnej, uzyskanie listy dodatkowych pytań raz lub więcej, zaproszenie do rundy odpowiedzi ustnych raz lub więcej, wycofanie aplikacji przez spółkę i jej ponowne złożenie po uzupełnieniach lub inne nieprzewidywane na tym etapie przez spółkę” — zastrzegał Mabion w komunikacie giełdowym z 28 stycznia, gdy złożył odpowiedzi na ostatnią rundę pytań EMA.
Analitycy PKO BP pod koniec ubiegłego roku obniżyli prawdopodobieństwo uzyskania przez Mabion rejestracji leku w UE z 95 do 85 proc., podtrzymywali jednak pozytywne nastawienie do spółki.