Sędzia Vivian Medinilla orzekła w piątek wieczorem, że konsumenci mają naukowe podstawy do twierdzenia, że Zantac, który był własnością różnych firm na przestrzeni lat, może powodować różne rodzaje nowotworów. Podkreśliła również, że spory dotyczące analiz ekspertów w zakresie ryzyka zdrowotnego mogą być właściwie rozstrzygane w trakcie procesów sądowych. Około 75 tys. konsumentów złożyło pozwy w Delaware przeciwko byłym producentom tego leku.
Orzeczenie jest poważnym ciosem dla Pfizera, GSK i innych byłych producentów Zantacu, którzy mieli nadzieję przekonać sędzię Medinillę, aby poszła ona śladem federalnego sędziego z Florydy, który odrzucił dowody na rakotwórczość jako niewiarygodne w 2022 roku. Sędziowie z Kalifornii i Illinois uznali jednak wiele z tych samych dowodów za wiarygodne, co skłoniło GSK i Pfizer do zawarcia niektórych ugód.
Firma GSK z siedzibą w Wielkiej Brytanii oświadczyła w sobotę, że nie zgadza się z orzeczeniem Medinilli i złoży apelację.
Pfizer poinformował natomiast, że jest zaangażowany w "tylko niewielką część" spraw w Delaware i nadal nie dostrzega znaczącego wpływu postępowań dotyczących Zantacu na swoją działalność. Firma również zapowiedziała, że złoży apelację w tej sprawie.
Byli użytkownicy Zantacu pozwali producentów leku na zgagę, twierdząc, że produkt wywołał raka piersi, żołądka, jelita grubego i innych narządów. Firmy GSK, Sanofi i Pfizer zawarły już niektóre ugody (w przypadku Pfizera dotyczyły one 10 tys. spraw), a orzeczenie Medinilli może skłonić je do kolejnych porozumień pozasądowych.
Zantac pojawił się na rynku USA jako lek na receptę w 1983 roku, a w 1995 roku przekształcił się on w dostępny bez recepty lek na zgagę. Firmy GSK i Warner Lambert opracowały Zantac we wspólnym przedsięwzięciu. Następnie lek był własnością kilku innych firm (m.in. Pfizera), aż w 2017 roku przejęło go Sanofi.
Pfizer z problemami: duże trudności amerykańskiego koncernu
Pfizer mierzy się obecnie z dużymi trudnościami. Wraz z zakończeniem pandemii spadło zapotrzebowanie na szczepionki, co zmusiło firmę do poszukiwania nowych produktów, aby zrekompensować straty.
Siedem miesięcy temu Pfizer zdecydował się przerwać prace nad nowym lekiem na odchudzanie z powodu częstych skutków ubocznych. Jak donosi agencja Bloomberg, było to poważne wyzwanie dla planów firmy związanych z rozwijaniem innowacyjnych leków. Ponad połowa uczestników badań musiała przerwać stosowanie eksperymentalnego leku z powodu częstych nudności i wymiotów.
Pfizer poinformował ponadto w środę, że eksperymentalna terapia genowa firmy, opracowana w celu leczenia dystrofii mięśniowej Duchenne'a (DMD), nie wykazała poprawy funkcji ruchowych u pacjentów w zaawansowanym etapie badania w porównaniu z placebo.
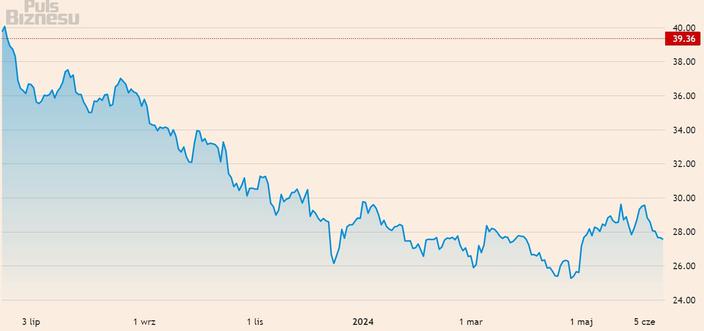
Od początku roku akcje Pfizera spadły o 30,7 proc., podczas gdy branża zanotowała wzrost o 28 proc.